Los compuestos de carbono
¿Cual es la importancia que tiene el carbono en la vida cotidiana?
Pues veras, el único elemento de la tabla periódica que puede conducir a la formación de millones de compuestos es el carbono, entre los cuales algunos constituyen a los sistemas vivientes. El carbono es un elemento que tiene muchos usos desde aplicaciones ornamentales del diamante en joyería hasta tintas de imprenta. Otra forma del carbono es el grafito, el cual se emplea en nuestros lapices.
Los compuestos de carbono se agrupan de la siguiente manera:
- Alifáticos: son compuestos de cadena abierta, cada átomo de cadena abierta se caracteriza por el numero de átomo de carbono a que va unido, se les denomina primarios, secundarios, y terciarios según este unido a 1, 2, o 3 átomos de carbono.
- Cíclicos: son compuestos de cadena cerrada. Si esta formada por solo átomos de carbono entonces se le denomina carbólico y si están combinadas con otros átomos como el nitrógeno, oxigeno, o azufre se les denomina policiclico.
- Aromáticos: son muy amplias, forma una familia de compuestos que tienen un núcleo en común, el benceno.
Estructura molecular de los compuestos de carbono
El carbono forma con el hidrógeno una gran cantidad de compuestos llamados hidrocarburos; en la composición del gas natural y del petróleo se encuentran diferentes tipos..El conocimiento de la estructura molecular de los compuestos es de gran importancia, ya que de ésta se derivan todas las propiedades de una sustancia, además son el punto de partida para su síntesis en el laboratorio y posteriormente en la industria, lo que constituye la base de muchas de las ramas de la técnica actual, que va desde la fabricación de nuevos plásticos, fibras sintéticas, nanomateriales hasta la de productos farmacológicos, todos basados en gran parte en los conocimientos en el análisis estructural.
Configuración electrónica del carbono
El carbono es una elemento que pertenece al periodo 2 y grupo 4 dentro de la tabla periódica. su numero atómico es 6 por lo tanto posee 6 protones 6 neutrones y electrones en su orbitales. Estos se distribuyen dos en dos entre los niveles 1s,2s y 2sp. su numero de masa es 12Según la gráfica orbital 1s y 2s están completamente ocupados, mientras que en el orbital p, aun le queda un sub-orbital por llenar,un orbital es el espacio que llega a ocupar dos electrones dentro de un mismo nivel.
Hibirdacion
Es la combinación de dos orbitales atómicos para formar un nuevo orbital molecular híbrido con características propias. Para describir la hibridacion del carbono debe tomar en cuenta que depende de su configuración electrónica que tenga cada átomo. El átomo de carbono se presenta en tres tipos de hibridaciones:- La hibridacion sp: Es la combinación orbital s y p para formar un orbital híbrido de forma lineal. Tiene un angulo de 180 grados entre los dos orbitales. Puede formar enlaces covalentes triples

Representación electrónica:
- La hibridacion sp^2: es la combinación orbital de un s y dos para formar tres orbitales híbridos en forma trigonal. tiene un angulo de separación de 120 grados entre los tres orbitales híbridos. Forma enlaces dobles covalentes.

- La hibridacion sp^3: es la combinación s y tres p para formar cuarto orbitales híbridos en forma tetraedrica. tiene un angulo de 109.5 entre los cuatro orbitales híbridos. Forma enlaces sencillos covalentes.

Representación electrónica:

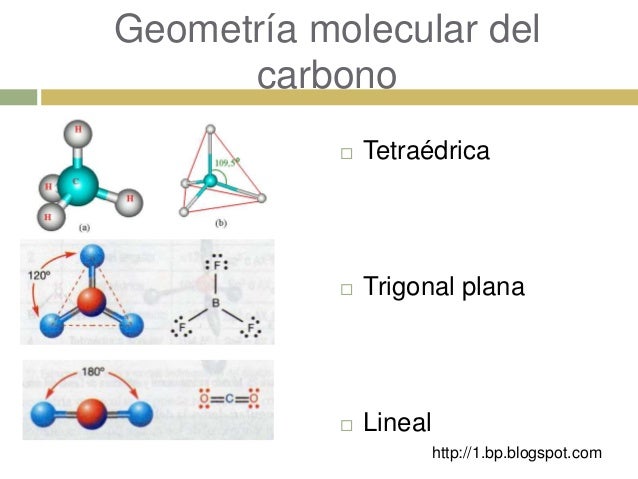
Geometría molecular del carbono
La geometría molecular significa la disposición tri-dimensional de los átomos que forman parte de un molécula. Determina muchas propiedades del las moléculas como la reactividad , polaridad, fase, color, magnetismo, actividad biológica etc. La geometría molecular del carbono puede ser:
- Tetraedrico: es cuando un átomo de carbono se una a cuatro átomos mediante enlaces covalentes
- Trigonal: es cuando se unan con tres átomos, estos se acomodan y se distribuyen en dirección de los vértices de un triangulo equilatero.
- Lineal: es cuando el átomo de carbono se una a solo a dos átomos, de tal manera que se distribución es lineal
Cadenas carbonadas e isomeros
Es el esqueleto de todos los compuestos orgánicos y esta formada por un conjunto de varios átomos de carbono, unidos entre si mediante enlaces covalentes carbono-carbono, y a la que se unen otros átomos como el hidrógeno, oxigeno, o nitrógeno formando variadas estructuras.Los isomeros de cadena poseen el mismo grupo funcional pero la estructura de la cadena es diferente,puede ser lineal, ramificada , etc. Las uniones entre los carbonos son a partir de cuatro átomos de carbono

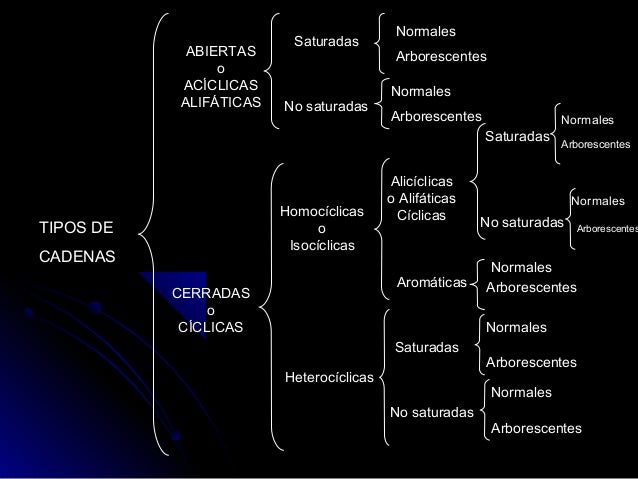
Descripción de los tipos de cadena carbonadas
Dado a que los átomos de carbono se pueden unir fácilmente entre si, su esqueleto básico de los compuestos orgánicos son cadenas de carbonos de diversas longitudes y formas. La longitud de la cadena determina el comportamiento químico de la sustancia.- Cadenas abiertas o acíclicas: es cuando las cadenas presentan dos extremos que son continuas.

- Cadenas homocíclicas: son cadenas carbonadas cerradas si todos los átomos que lo constituyen el anillo son carbonos. Los anillos se clasifican en alicíclicos y aromáticos. Los alicíclicos son propiedades similares a de una cadena abierta. Las cadenas aromáticos están relacionadas con el benceno y la mayoría tiene un olor agradable.

- Las cadenas heterocíclicas: se forman cuando uno de los átomos de carbono del anillo se encuentra sustituido por otro elemento como el
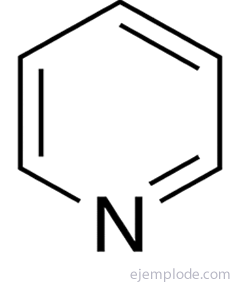
- Cadenas abiertas heterogéneas: es cuando los átomos que constituyen una cadena abierta participan otros elementos distintos que el carbono (oxigeno o nitrógeno).


- Cadenas sencillas o ramificadas: cuando las cadenas carbonadas no tienen ramificaciones se les llama sencillas. Cuando las cadenas carbonadas presentan ramificaciones entonces se les denomina ramificadas o arborescentes.
Representación de las moléculas orgánicas
Para diferenciar entre los compuestos de carbono se utilizan formulas semi-desarrollada y desarrollada o estructural.estas formulas fueron utilizadas por el quimico Irving Langmuir, por se les llama formulas de Langmuir.- Formula semi-desarrolllada: es la mas utilizada porque en ella se detallan algunos enlaces los que estan presentes entre el carbono lo que ayuda diferenciar unos compuestos de otros. cuando esta cadena es muy larga, su formula semidesarrollada se abrevia utilizando parentesis y subindice.
- Formula se taquigrafica: los enlaces se presentan mediante lineas ascendentes y descendentes de forma triangular.los vertices indican el numero de atomos de carbono e hidrogeno.
- Formula desarrollada o estructural: en ellas se indican todos los enlace que forman una molecula.
| Formula estructural |
 |
| Formula taquifrafica |
 |
| Formula semi-desarrollada |